Hochaufgelöste Struktur und Dynamik des mitochondrialen Komplexes I
Die Versorgung der Zellen mit Energie gilt als essenzieller Prozess in allen Formen des Lebens. Der Atmungskomplex I spielt eine zentrale Rolle im aeroben Energiestoffwechsel, aber sein molekularer Mechanismus war bisher noch weitgehend unverstanden. In einer neuen Studie mit Hilfe von Kryo-Elektronenmikroskopie und Computersimulationen haben Forschende des Max-Planck-Instituts für Biophysik und der Goethe-Universität Frankfurt zusammen mit Kollegen der Universität Helsinki die hochauflösende Struktur und Dynamik der katalytischen Funktion dieser Schlüsselkomponente der biologischen Energieumwandlung aufgezeigt.
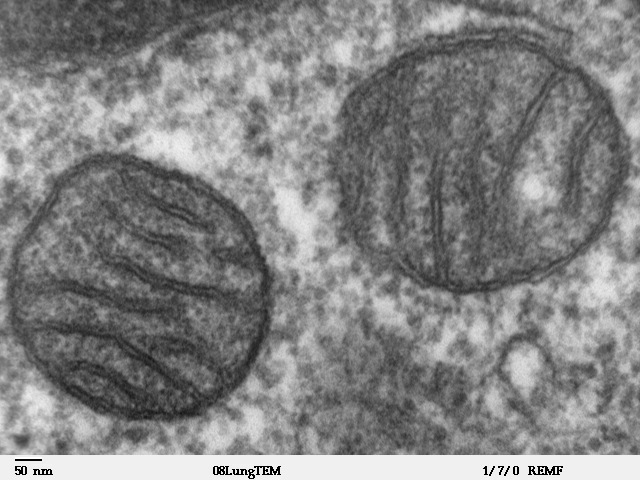
Mitochondrien: Besonders viele befinden sich in Zellen mit hohem Energieverbrauch; unter anderem Muskelzellen, Nervenzellen, Sinneszellen und Eizellen. In Herzmuskelzellen erreicht der Volumenanteil von Mitochondrien 36 %. Sie haben einen Durchmesser von etwa 0,5–1,5 µm und sehr unterschiedliche Formen, von Kugeln bis zu komplexen Netzwerken. Mitochondrien vermehren sich durch Wachstum und Sprossung, ihre Anzahl von Mitochondrien wird dem Energiebedarf der Zelle angepasst. – Elektronenmikroskopische Aufnahme © Louisa Howard, gemeinfrei
Alle Lebensprozesse erfordern eine ständige Versorgung mit Energie. ATP (Adenosintriphosphat) wird in spezialisierten Organellen der Zelle, den Mitochondrien, gebildet und dient als molekularer Treibstoff der Zelle. Der mitochondriale Komplex I (auch NADH:Ubiquinon Oxidoreduktase) ist ein sehr großer, 1-MDa-Membranproteinkomplex; er bildet den Ausgangspunkt der mitochondrialen Atmungskette, die die treibende Kraft für die ATP-Synthese liefert.
Die mitochondriale NADH:Ubichinon-Oxidoreduktase (Komplex I) ist der größte und komplizierteste Membranproteinkomplex der Atmungskette. Komplex I koppelt die Übertragung von Elektronen aus reduziertem Nicotinamid-Adenin-Dinukleotid (NADH) auf Ubichinon mit der Verlagerung von Protonen durch die innere Mitochondrienmembran.
Das Forscherteam hat neue Erkenntnisse über die Funktionsweise von Komplex I gewonnen: Mit Hilfe der Kryo-Elektronenmikroskopie konnten sie seine 3D Struktur mit bisher unerreichter Auflösung bestimmen. Protonentransfer-Reaktionen entlang von Wassermolekül- und bestimmten Aminosäure-Ketten spielen eine zentrale Rolle für die Funktion von Komplex I. Die exzellente Qualität der Strukturdaten ermöglichte es, Wassermoleküle in der Proteinstruktur genau zu lokalisieren und Rückschlüsse auf Protonentransferwege zu ziehen. Diese Strukturdaten ermöglichten auch umfangreiche Computersimulationen, die neue Einblicke in die Dynamik des Komplexes geben. Die Ergebnisse sind in Science Advances veröffentlicht worden und liefern ein neues und detailliertes Bild davon, wie eine molekulare Maschine funktioniert.
->Quellen und mehr:
- biophys.mpg.de/news_publication_17879994_transferred
- Originalpublikation: Kristian Parey, Jonathan Lasham, Deryck J. Mills, Amina Djurabekova, Outi Haapanen, Etienne Galemou Yoga, Hao Xie, Werner Kühlbrandt, Vivek Sharma, Janet Vonck and Volker Zickermann: High-resolution structure and dynamics of mitochondrial complex I—Insights into the proton pumping mechanism, in: Science Advances, 12 Nov 2021, Vol 7, Issue 46, DOI: 10.1126/sciadv.abj32, open access
- science.org/doi/epdf/10.1126/sciadv.abj3221
- pure.mpg.de/ViewItemFullPage.jsp