Kohlenstoffpellets als Grundmaterie
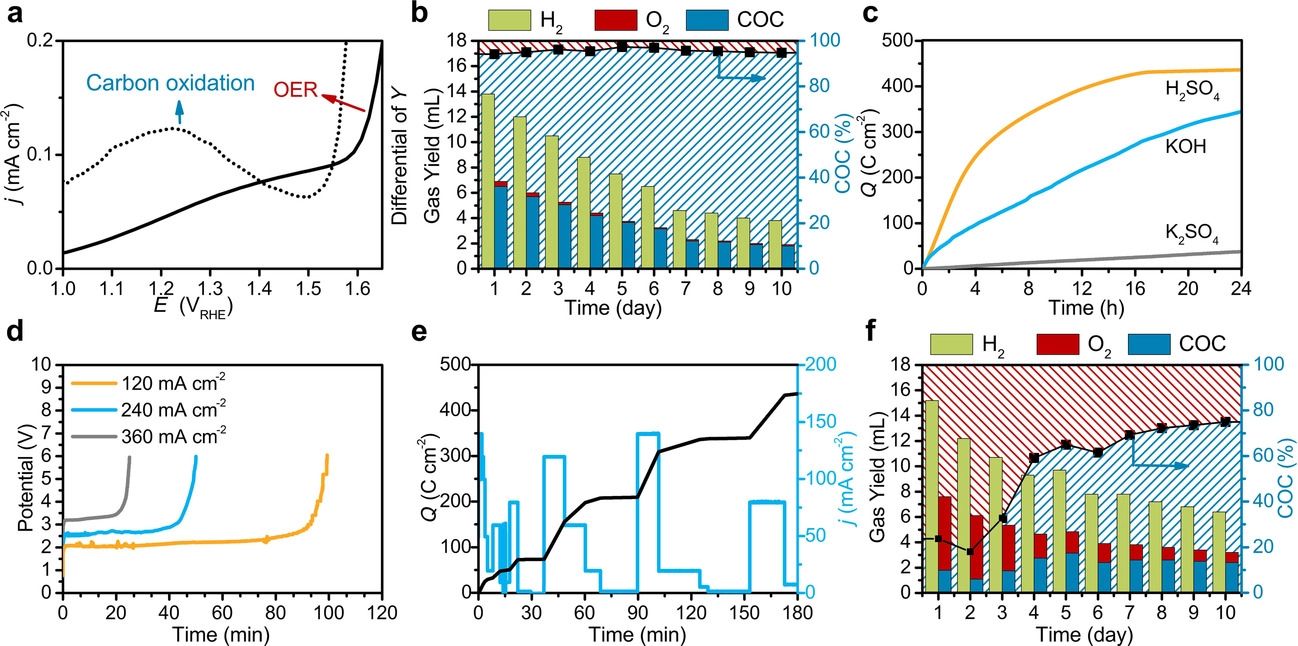
a) Strom-Potenzial-Kurve eines Kohlenstoffs als Elektrode und die relative Differenzkurve (gestrichelte Linie). b) Tägliche Gassammlung in einer Zelle mit zwei Elektroden: Wasserstoff an der Kathode; Sauerstoff und der Kohlenstoffoxidationsbeitrag (COC) an der Anode. Rot schraffierte Bereiche zeigen die Wasserstoffproduktion aus der Wasseroxidation (katalytischer Prozess), während blau schraffierte Bereiche die Wasserstoffproduktion aus der Kohlenstoffoxidation darstellen. c) Ladungssammlung des Kohlenstoffpellets in sauren (H2SO4, pH 1), alkalischen (KOH, pH 13) und neutralen (K2SO4, pH 7) Elektrolyten. d) Stabilität der Kohlenstoffpellets in 1 m KOH bei Stromdichten von 120, 240 und 360 mA/cm2. e) Leistung des Kohlenstoffpellets unter dynamischen Potenzialschwankungen zur Nachahmung der Flexibilität von solar abgeleitetem Strom. f) Tägliche Gassammlung des stickstoffhaltigen Kohlenstoffpellets in einer Zwei-Elektroden-Zelle – Grafiken © chemistry-europe.onlinelibrary.wiley.com – CC-BY 4.0
Pflanzliche Biomasse wurde bereits zur Herstellung kostengünstiger kohlenstoffhaltiger Materialien verwendet, was die Möglichkeit einer großtechnischen Produktion demonstriert. Um eine skalierbare, unabhängige und langfristige Anwendung zu ermöglichen, wurde eine Technik entwickelt, bei der der pulverförmige Kohlenstoff ohne Bindemittel zu Pellets gepresst wird. Die elektrochemischen Tests mit den Kohlenstoffpellets wurden in einer Zwei-Elektroden-Zelle durchgeführt, und die gasförmigen Produkte wurden gesammelt. Die Kathodenseite erzeugte kontinuierlich Wasserstoff, während die Anodenseite eine geringe Menge Sauerstoff produzierte. Das Hauptprodukt an der Anodenseite war CO2, das direkt im Elektrolyten in Form von Karbonat gelöst wurde. Karbonat kann von MS direkt nachgewiesen werden. Im Allgemeinen ist die Wiederverwertung des reinen CO2 aus dem Elektrolyten viel einfacher als die Kontrolle des Treibhausgases aus der fossilen Verbrennung aus der Atmosphäre, das mit einer ganzen Reihe anderer Gase vermischt ist. Der Beitrag der katalytischen Produktion war stabil bei etwa 5 % im Vergleich zum Beitrag der Kohlenstoffoxidation (COC), der sich bei 95 % einpendelte. Die Gesamtgasproduktion ging aufgrund des Verbrauchs und der Ablösung kleiner Kohlenstofffragmente vom Pellet zurück. Die Lebensdauer einer Elektrode im industriellen Maßstab sollte mehrere tausend Stunden betragen und würde eine kontinuierliche Speisung der Opferelektrode erfordern…
Aus Biomasse gewonnene Kohlenstoffelektrode mit großem Potenzial
Zusammenfassend wird ein chemisches Energieumwandlungskonzept zur Verwendung von Kohlenstoff-Opferelektroden für die Umwandlung von solar gewonnener Elektrizität in Wasserstoff durch Wasserspaltung vorgeschlagen. Die anodische, aus Biomasse gewonnene Kohlenstoffelektrode kann entweder die klassische katalytische Wasseroxidation oder eine Selbstoxidation erfüllen. Die technische Machbarkeit wird in verschiedenen Elektrolyten und unter industriell relevanten Bedingungen hoher, dynamischer Ströme demonstriert. Die Aussicht auf eine chemische Modifikation zeigt ein großes Potenzial zur Verbesserung der Elektroden-Lebensdauer. Anstatt Kohlenstoff als direkten Energieträger zu verwenden, bietet die Anwendung von Kohlenstoff als Opferelektrode eine industriell saubere, skalierbare und nachhaltige Idee zur Gewinnung von „grünem“ Wasserstoff.
->Quelle und mehr:
- cec.mpg.de/elektrode-auf-kohlenstoffbasis-zur-wasserstoffproduktion
- Originalpublikation: Ding, Y., Greiner, M., Schlögl, R., Heumann, S. (2020). A Metal-Free Electrode: From Biomass-Derived Carbon to Hydrogen – in: ChemSusChem – https://doi.org/10.1002/cssc.202000714 – CC-BY 4.0
- Teils übersetzt mit DeepL.com/Translator